15 December 11th Chemistry Question Paper Half Yearly Exam 2025
| Subject | Chemistry |
| Session | 2025-26 |
| Exam Date | 15.12.2025 |
| WhatsApp Channel | Join Now |
| YouTube Channel | Click Here |
Bihar Board 11th Half Yearly Exam 2025-26
जितने भी छात्र-छात्राएं वार्षिक परीक्षा 2026 में सम्मिलित होने जा रहे हैं। उसे पहले उनको दिसंबर महीने में अर्धवार्षिक परीक्षा देना होगा।
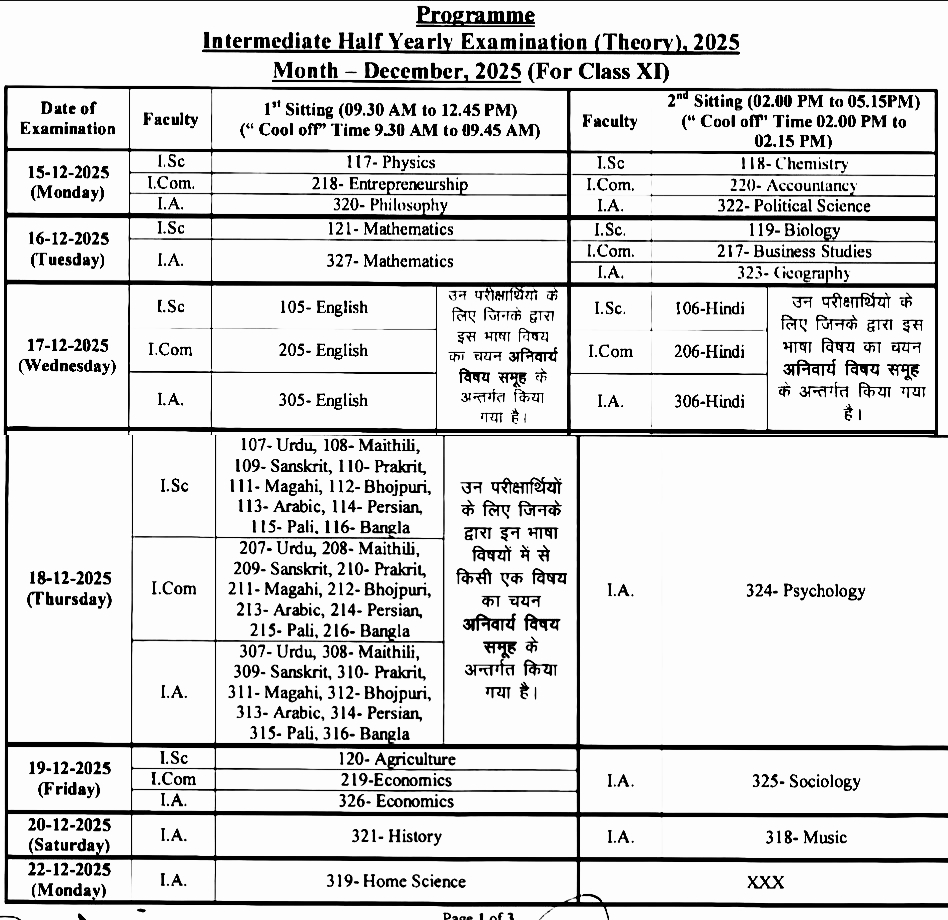
Class 11th Exam Routine Half Yearly Exam 2025
कितने सिलेबस से प्रश्न रहेंगे Half Yearly Exam 2025 Syllabus
कक्षा 11th के अर्धवार्षिक परीक्षा 2025 का प्रश्न पत्र आपके विद्यालय में नवंबर माह तक पढ़ाए गए पाठ से प्रश्न आएगा
इस परीक्षा में फेल करने पर क्या होगा ?
यह विद्यालय के स्तर पर आयोजित होने वाली अर्धवार्षिक परीक्षा है। इसलिए इस परीक्षा में भाग लेना अनिवार्य है
अर्धवार्षिक परीक्षा Exam 2025-EXAM CENTER
इस परीक्षा का आयोजन आपके विद्यालय के स्तर पर होगा। अर्थात की जिस भी विद्यालय में आपका नामांकन है। उसी में जाकर आपको परीक्षा देना पड़ेगा ।
क्या अर्धवार्षिक परीक्षा के कॉपी Check होता हैं?
जी हां, जब आपकी परीक्षा सम्पन्न हो जाती हैं, तब आपके कॉपी को आपके विद्यालय/कॉलेज के शिक्षकों के द्वारा चेक की जाती हैं।
अर्धवार्षिक परीक्षा का महत्व
यदि आप भी 11th का अर्धवार्षिक परीक्षा देने जा रहे हैं या देने वाले हैं तो आप सभी को इस परीक्षा में भाग लेना अति आवश्यक है अर्धवार्षिक परीक्षा का उद्देश्य छात्रों की आगे की कक्षा में प्रवेश करने से पहले उसकी तैयारी को जांच किया जाए और तैयारी को बेहतर किया जाए ताकि वह आगे परीक्षा में किसी भी प्रकार में उनको दिक्कत ना हो और उनको जो भी कमजोरी है वह उसको सुधार सके इसलिए अर्धवार्षिक परीक्षा लिया जाता है
Class 11th Chemistry Objective Answer Key 2025
| 1.A | 11.B | 21.B | 31.C | 41.B |
| 2.A | 12.B | 22.C | 32.B | 42.D |
| 3.B | 13.D | 23.B | 33.B | 43.B |
| 4.D | 14.A | 24.C | 34.C | 44.A |
| 5.B | 15.C | 25.A | 35.C | 45.B |
| 6.D | 16.B | 26.C | 36.B | 46.B |
| 7.C | 17.B | 27.B | 37.B | 47.A |
| 8.B | 18.B | 28.B | 38.A | 48.D |
| 9.C | 19.B | 29.C | 39.A | 49.A |
| 10.C | 20.B | 30.A | 40.D | 50.C |
Download Subjective Question
1. मोल को परिभाषित करें । / Define mole.
उत्तर- एक मोल होता है, जैसे एक दर्जन, जिसमें दोनों ही विशुद्ध संख्याएं हैं, जिनमें कोई भी इकाई नहीं है। यह किसी भी प्रकर के मूलभूत पदार्थ की व्याख्या कर सकता है, (पदार्थ जो परमाणु से बना हो)। मोल का प्रयोग केवल आण्विक्, परमाण्विक और अन्तर-आण्विक कणों के मापन तक ही सीमित है।
2. गैसीय आयतन का नियम क्या है ? / What is the law of gaseous volume ?
उत्तर- नियम कहता है कि जब भी गैसें एक साथ क्रिया करती हैं तो वे ऐसे आयतन के संयोजन में करती हैं जिसमें वे एक दूसरे के लिए एक सरल पूर्ण-संख्या अनुपात और उत्पादों के साथ भी होते हैं यदि वे गैसीय रूप में होते हैं।
3. ऑक्सीकारक और अपचायक एजेंटों के दो-दो उदाहरण दीजिए। / Give two examples each of oxidizing
उत्तर- वे पदार्थ जिनका ऑक्सीकरण होता है तथा ये इलेक्ट्रॉन त्यागकर दूसरे पदार्थ को अपचयित करते हैं, उन्हें अपचायक कहते हैं | वे पदार्थ जिनका अपचयन होता है तथा इलेक्ट्रॉन ग्रहण कर दूसरे पदार्थ को ऑक्सीकृत करते हैं, उन्हें ऑक्सीकारक कहते हैं | अतः अपचायक इलेक्क्ट्रॉनदाता तथा ऑक्सीकारक इलेक्ट्रॉनग्राही होता है।
4.न्यूलैंड का अष्टक नियम क्या है?
उत्तर – न्यूलैंड के अष्टक नियम के अनुसार हर आठवां तत्व पहले तत्व के गुणधर्म के बराबर है। साल 1864 में वैज्ञानिक जॉन एलेक्जेंडर न्यूलैंडस ने जब रासयनिक तत्वों को बढ़ते क्रम में उनके परमाणु भार के अनुसार व्यवस्थित किया, तब उन्हें समझ आया की हर 8वां तत्व पहले तत्व के अनुसार ही गुण रखता है।
5.इलेक्ट्रॉनों की निर्जन जोड़ी से आप क्या समझाते हैं?
उत्तर – इलेक्ट्रॉन की निर्जन जोड़ी इलेक्ट्रॉनों का ऐसा जोड़ा जो सहसंयोजन बंधन के बनने में भाग नहीं लेता है। इलेक्ट्रॉन की निर्जन जोड़ी कहलाता है। उदाहरण के लिए, जल (H2O) के बनने में ऑक्सीजन परमाणु के पास दो जोड़े इलेक्ट्रॉन शेष रह जाते हैं, जिनका साझा किसी भी परमाणु के साथ नहीं होता है।
6. किसी द्रव के वाष्प दाब से आप क्या समझते हैं?
उत्तर – किसी द्रव का वाष्प-दाब, द्रव की प्रकृति तथा ताप पर निर्भर करता कोई अवाष्पशील द्रव या ठोस, द्रव विलायक में मिलाया जाता है तो द्रव विलायक का वाष्प – दाब कम हो जाता है क्योंकि विलयन में द्रव की सतह पर विलायक के अणुओं की संख्या शुद्ध विलायक की तुलना में कम हो जाती है।
7. स्थिर ताप पर गैस के दाब एवं घनत्व में क्या संबंध है ?
उत्तर: स्थिर ताप पर, गैस का दाब और घनत्व व्युत्क्रमानुपाती होते हैं। इसका मतलब है कि यदि गैस का दाब बढ़ता है, तो गैस का घनत्व कम होगा, और यदि गैस का दाब कम होता है, तो गैस का घनत्व बढ़ेगा।
8. अम्ल एवं क्षारक संबंधी लुईस के सिद्धान्त को लिखें।
उत्तर: यह सिद्धान्त बताता है कि अम्ल यह पदार्थ होता है जो इलेक्ट्रॉन युग्म स्वीकार कर सकता है, और क्षारक वह पदार्थ होता है जो इलेक्ट्रॉन गुग्म दान कर सकता है।
9. जल की कठोरता से आप क्या समझते हैं?
उत्तर: जल में उपस्थित कैल्शियम और मैग्नीशियम आयनों की माया को दर्शाता है। जल में इन आयनों की अधिक मात्रा जम को कठोर बनाती है।
(10) अपचयन को परिभाषित करें।
उत्तर- अपचयन का मतलब एक ऐसी अभिक्रिया होता है, जिसमे हाइड्रोजन या किसी अन्य विद्युत् धनात्मक तत्त्व का संयोग हो या फिर ऑक्सीजन अथवा विद्युत् ऋणात्मक तत्त्व का वियोग हो।
11.औफबाउ का सिद्धांत क्या है ? / What is Aufbau’s principle
उत्तर- आफबाऊ’ एक जर्मन शब्द है जिसका अर्थ है- ‘एक-एक कर जोड़ना’। इस सिद्धान्त के अनुसार, किसी कक्षा तथा उपकक्षा में इलेक्ट्रॉनों का प्रवेश ऊर्जा स्तरों के बढ़ते ऊर्जा के क्रम में एक-एक कर होता है।
12.किसी विलयन की मोलरता और मोललता के बीच क्या अंतर है ? / What is the difference between
उत्तर- मोलरता (molarity of solution) — विलयन के एक लीटर में विलीन विलेय (sotute) के मोलो की संख्या विलयन की मोलरता कहलाती हैं। मोललता (molality of solution) – 1 किलोग्राम विलायक में विलीन विलेय के मोलों कि संख्या विलयन की मोललता कहलाती हैं।
13. प्रेरणिक प्रभाव से आप क्या समझते हैं? यह कितने प्रकार का होता है ? उदाहरण दें।
उत्तर: एक ऐसा प्रभाव है जो किसी परमाणु या अणु में उपस्थित इलेक्ट्रॉनों के वितरण को विकृत कर देता है। यह विकृति इलेक्ट्रॉनों के धनत्व में परिवर्तन लाती है, जिसके परिणामस्वरूप ध्रुवीयता उत्पन्न होती है।
प्रेरणिक प्रभाव दो प्रकार का होता है
धनात्मक प्रेरणिक प्रभावः जब कोई इलेक्ट्रॉन-आकर्षक परमाणु किसी इलेक्ट्रॉन-प्रतिकर्षी परमाणु से जुड़ा होता है, तो इलेक्ट्रॉन घनत्व इलेक्ट्रॉन-आकर्षक परमाणु की और सीच जाला है। ऋणात्मक प्रेरणिक प्रभावः जब कोई इलेक्ट्रॉन-प्रतिकी परमाणु किसी इलेक्ट्रॉन-आकर्षक परमाणु से जुड़ा होता है, तो इलेक्ट्रॉन घनत्व इलेक्ट्रॉन प्रतिकर्षी परमाणु से दूर खींच जाता है।
उदाहरण
धनात्मक प्रेरणिक प्रभावः HCL में, C. परमाणु । परमाणु की तुलना में अधिक इलेक्ट्रॉन आकर्षक होता है। इसलिए, इलेक्ट्रॉन घनत्व ८. परमाणु की ओर खींच जाता है, जिसके परिणामस्वरूप HCI ध्रुवीय हो जाता है।
14.औफबाउ का सिद्धांत क्या है ?
उत्तर- आफबाऊ’ एक जर्मन शब्द है जिसका अर्थ है- ‘एक-एक कर जोड़ना’। इस सिद्धान्त के अनुसार, किसी कक्षा तथा उपकक्षा में इलेक्ट्रॉनों का प्रवेश ऊर्जा स्तरों के बढ़ते ऊर्जा के क्रम में एक-एक कर होता है।
(15) ऑक्सीकरण क्या है ?
उत्तर- ऑक्सीकरण अभिक्रिया में किसी तत्त्व या यौगिक से ऑक्सीजन का संयोजन अथवा किसी यौगिक से हाइड्रोजन का निष्कासन होता है। इसका सबसे अच्छा उदाहरण है जब कार्बन को ऑक्सीजन की उपस्थिति में या वायु की उपस्थिति में जलाया जाता है तो वह ऑक्सीजन से संयोग कर कार्बन डाइऑक्साइड गैस का निर्माण करता है।
(16) अपचयोपचय अभिक्रियाएं क्या है ?
उत्तर – अपचयोपचय अभिक्रिया (Redox Reaction) ऑक्सीकरण तथा अपचयन की अभिक्रियाओं में यह पदार्थ जो इलेक्ट्रॉन देता है उसका ऑक्सीकरण होता है तथा पदार्थ जो इलेक्ट्रॉन ग्रहण करता है उसका अपचयन होता है तथा इस सम्पूर्ण अभिक्रिया को अपचयोपचय (रेडोक्स अभिक्रिया) अभिक्रिया कहते हैं।
(17) ऑक्सीकरण अवस्था से आप क्या समझते हैं ?
उत्तर- इलेक्ट्रॉन ऋणात्मकता को ध्यान रखते हुए एक विशेष यौगिक में तत्व के किसी परमाणु द्वारा अन्य परमाणु के आवेश की संख्या ग्रहण करने को उसकी ऑक्सीकरण अवस्था कहते है।
(18) उदाहरण के साथ ऑक्सीकारक को परिभाषित करें।
उत्तर- वह अभिकर्मक जो किसी पदार्थ का ऑक्सीकरण करता है अर्थात् उसके ऑक्सीकरण अंक में वृद्धि करता है, ऑक्सीकारक कहलाता है। जैसे – 2Na+Cl2→2NaCl में C12 ऑक्सीकारक है।
19.व्युत्क्रम अनुपात का नियम क्या है? एक उदाहरण देकर व्याख्या करें।
उत्तर – व्युत्क्रम अनुपात के नियम के अनुसार जब हाइड्रोजन व ऑक्सीजन परस्पर संयोग करेंगे तो उनके द्रव्यमानों का अनुपात यही होगा अथवा इसका सरल गुणक होगा। हाइड्रोजन व ऑक्सीजन के परस्पर संयोग से बने जल (H2O) में इन दोनों तत्वों का भारात्मक अनुपात 1:8 ही होता है।
20.डाल्टन का परमाणु सिद्धांत क्या है
उत्तर – सन 1808 में वैज्ञानिक जॉन डाल्टन नए प्रयोगों के आधार पर एक सिद्धांत प्रस्तुत किया। जिसे डाल्टन का परमाणु सिद्धांत (Dalton atomic theory) कहते हैं। डाल्टन ने इस सिद्धांत के कुछ महत्वपूर्ण तथ्य प्रस्तुत किए जो निम्न प्रकार से हैं।
21. द्रव्य अति सूक्ष्म अविभाज्य कणों से मिलकर बना होता है। जिसे परमाणु कहते हैं।
2. एक तत्व के सभी परमाणु आकार, आकृति तथा द्रव्यमान आदि गुणों में समान होते हैं। जबकि भिन्न- भिन्न तत्वों के परमाणु इन गुणों में भिन्न भिन्न होते हैं।
3. परमाणु को न तो उत्पन्न किया जा सकता है और न ही नष्ट किया जा सकता है।
4. एक से अधिक तत्वों के परमाणु निश्चित अनुपात में संयोजित होकर यौगिक/अणु बनाते हैं।
5. दो तत्वों के परमाणु गुणों में एक दूसरे से भिन्न भिन्न होती हैं। एवं उनके परमाणु भार, आकार आदि भिन्न- भिन्न होते हैं।
2.मैक्स प्लांक क्वांटम सिद्धांत क्या है
उतर – इस सिद्धांत के अनुसार, विद्युत चुंबकीय विकरणों का उत्सर्जन (अवशोषण) सतत न होकर ऊर्जा के छोटे- छोटे पैकटों अथवा बंडलों के रूप में होता है। इन ऊर्जा के पैकेटों को फोटोन या क्वांटम कहते हैं। एवं इस सिद्धांत को मैक्स प्लांक का क्वांटम सिद्धांत (Max Planck Quantum theory) कहते हैं।
इस सिद्धांत के प्रमुख तथ्य निम्न प्रकार से हैं।
• ऊर्जा का अवशोषण या उत्सर्जन ऊर्जा के छोटे-छोटे पैकेटों के रूप में होता है।
• प्रत्येक फोटोन (क्वांटम) की ऊर्जा E तथा आवृत्ति v (न्यू) होती है जो उसकी ऊर्जा के समानुपाती होती है।
22.आधुनिक आवर्त सारणी की विशेषताएं लिखें
उत्तर _
1. इसमें तत्वों को उनके परमाणु क्रमांकों के बढ़ते हुए क्रम में व्यवस्थित किया गया है।
2. आवर्त सारणी में 9 वर्ग हैं जो से VIII तथा शून्य वर्ग में व्यवस्थित हैं।
3. एक वर्ग में तत्वों के गुणों की समानता होती है। तथा दूसरे वर्ग से गुणों में भिन्न होते हैं।
4. आवर्त सारणी में कुल 7 आवर्त हैं। जो संख्या 1 से 7 तक हैं।
5. इसमें ऊर्ध्वाधर स्तंभों को वर्ग कहते हैं। इनकी संख्या कुल 9 होती है।
6. आवर्त सारणी में क्षैतिज पंक्तियों को आवर्त कहते हैं इनकी कुल संख्या 7 होती है।
